金沙集团1862cc生物医学光子学研究中心屈军乐教授团队和新加坡国立大学刘小刚教授合作,在光学超分辨成像领域取得重要进展,研究成果发表在Angew. Chem.(IF:12.257,中科院JCR 1区,TOP期刊)上,论文题目为《Designing Sub-2 nm Organosilica Nanohybrids for Far-Field Super-Resolution Imaging》(DIO: 10.1002/anie.201912404)。助理教授严伟为文章共同一作,屈军乐教授和新加坡国立大学刘小刚教授为论文共同通讯作者。
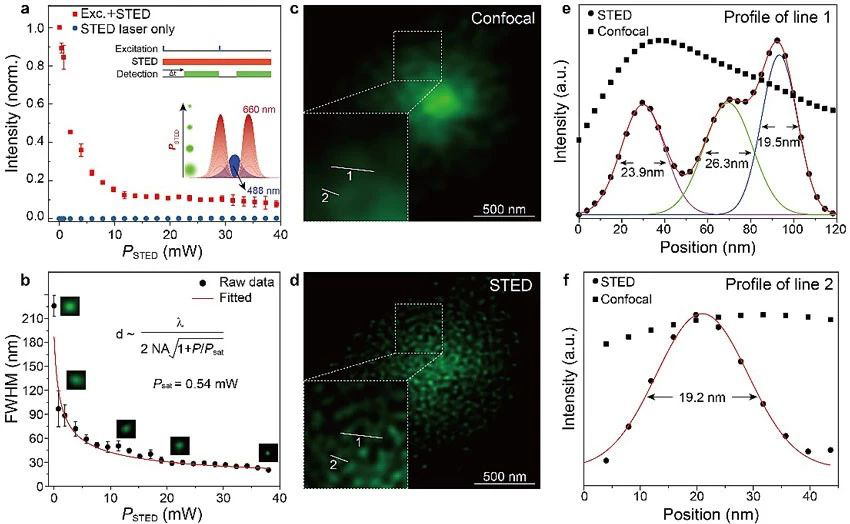
受激辐射损耗(Stimulated-emission depletion,STED)光学超分辨成像技术自上世纪90年代发明以来,已经在众多领域,包括微纳加工、高密度信息存储,尤其是细胞成像等方面取得重要进展,并荣获2014年度诺贝尔化学奖。在实际应用中,荧光标记物的众多理化性质(比如光稳定性、荧光抑制难易程度、尺寸、生物相容性、水溶性等)决定了最终超分辨成像的应用效果。近年来,除传统荧光分子之外,科学家开发了众多类型的纳米荧光标记物,比如半导体量子点、碳量子点、AIE纳米颗粒、半导体纳米颗粒、上转换纳米颗粒等。尽管这些荧光标记物可以在某些方面表现出优异的性能,但都具有一些先天性的缺陷,比如重金属毒性、物理尺寸过大或者荧光抑制效果较差等。最近,金沙集团1862cc和新加坡国立大学(NUS)的团队合作,发展了一种基于有机硅杂化荧光纳米点的STED荧光标记物。这种新型的STED荧光纳米点具有超小的物理尺寸(< 2 nm)和约100%的荧光量子产率,并且表现出极其优异的超分辨性能(如图所示)。
全文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/anie.201912404
此外,金沙集团1862cc生物医学光子学研究中心近年来在STED超分辨成像方面发展了一系列新的改进方法和手段,用于提高STED的成像性能,并探索新的应用,取得了重要的进展。首次将相干自适应光学(COAT)技术引入STED,极大的提高了STED的成像深度以及厚样品成像的空间分辨率,研究成果发表在Photonics Research(2017, 5(3):176. IF:5.522,中科院JCR 1区,TOP期刊)上。引入遗传算法,提高了AO像差校正的速度和精度,实现快速实时像差校正STED成像,研究成果发表在Nanophotonics(2018,7(12):1971. IF:6.908,中科院JCR1区,TOP期刊)上。首次将钙钛矿量子点用于STED成像,显著提高了探针的抗光漂白性能,实现了20nm的超高分辨率,研究结果发表在Advanced Materials(2018,30:1800167. IF:25.809,中科院JCR1区,TOP期刊)上。发展了一种新型碳点作为STED探针,在STED超分辨成像过程中,碳点表现出优异的超分辨特性,其在活细胞成像中能达到19.7nm的超高分辨率,同时具有较好的光稳定性和优秀的生物相容性,相关结果发表在Nano Research(IF:8.515中科院JCR1区)上
(论文链接:https://doi.org/10.1007/s12274-019-2554-x)
另外,该团队还通过寿命调控、相图分析等手段,发展了用于降低激发光功率,提高空间分辨率的方法,研究结果发表在Journal of Biophotonics(2018,e201800315.IF:3.763中科院JCR2区), Nanoscale(2018,10: 16252-16260, IF:6.97,中科院JCR1区,TOP期刊)以及Laser & Photonics Reviews(accepted)上。
以上工作得到了973计划、国家重点研发计划、国家自然科学基金、广东省和深圳市基金项目的支持。


![]() 地址:金沙集团1862cc沧海校区致原楼
地址:金沙集团1862cc沧海校区致原楼 ![]() 邮箱 :cpoe@szu.edu.cn
邮箱 :cpoe@szu.edu.cn ![]() 电话 :0755-26538735
电话 :0755-26538735 ![]() 传真 :0755-26538735
传真 :0755-26538735